അമോണിയം നൈട്രേറ്റ്
NH
4NO
3 എന്ന രാസ സൂത്രവാക്യമുള്ള ഒരു രാസ സംയുക്തമാണ് അമോണിയം നൈട്രേറ്റ് ( NH
4NO
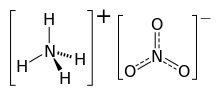
3 ). അമോണിയം, നൈട്രേറ്റ് എന്നിവയുടെ അയോണുകൾ അടങ്ങിയ ഒരു വെളുത്ത ക്രിസ്റ്റലിൻ ഖരമാണിത് . ഖരരൂപത്തിൽ ഹൈഗ്രോസ്കോപ്പിക് ആയി കാണപ്പെടുന്ന ഇത് ജലത്തിൽ വളരെയധികം ലയിക്കുന്നു. പ്രധാനമായും നൈട്രജൻ വളമായി കാർഷിക മേഖലയിലാണ് ഇത് ഉപയോഗിക്കുന്നത്. [4]
| |

| |

| |
| Names | |
|---|---|
| IUPAC name
Ammonium nitrate
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.026.680 |
| EC Number |
|
PubChem CID
|
|
| RTECS number |
|
| UNII | |
| UN number | 0222 – with > 0.2% combustible substances 1942 – with ≤ 0.2% combustible substances 2067 – fertilizers 2426 – liquid |
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | white/grey solid |
| സാന്ദ്രത | 1.725 g/cm3 (20 °C) |
| ദ്രവണാങ്കം | |
| ക്വഥനാങ്കം | |
| Endothermic 118 g/100 ml (0 °C) 150 g/100 ml (20 °C) 297 g/100 ml (40 °C) 410 g/100 ml (60 °C) 576 g/100 ml (80 °C) 1024 g/100 ml (100 °C)[1] | |
| -33.6·10−6 cm3/mol | |
| Structure | |
| trigonal | |
| Explosive data | |
| Shock sensitivity | very low |
| Friction sensitivity | very low |
| Hazards | |
| Main hazards | Explosive, Oxidizer |
| GHS pictograms |   
|
| GHS Signal word | Danger |
| H201, H271, H319 | |
| P220, P221, P271, P280, P264, P372 | |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
2085–5300 mg/kg (oral in rats, mice)[2] |
| Related compounds | |
| Other anions | Ammonium nitrite |
| Other cations | Sodium nitrate Potassium nitrate Hydroxylammonium nitrate |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
ഖനനം, ക്വാറി, നിർമ്മാണമേഖലയിൽ ഉപയോഗിക്കുന്ന സ്ഫോടനാത്മക മിശ്രിതങ്ങളുടെ ഘടകമാണ് ഇതിന്റെ മറ്റൊരു പ്രധാന ഉപയോഗം. വ്യാവസായിക സ്ഫോടകവസ്തുക്കളായ ANFO യുടെ പ്രധാന ഘടകമാണിത്.
ദുരുപയോഗത്തിനുള്ള സാധ്യതയെക്കുറിച്ചുള്ള ആശങ്കകൾ കാരണം പല രാജ്യങ്ങളും ഇത് ഉപയോഗിക്കുന്നത് നിർത്തലാക്കുന്നു. ആകസ്മികമായ അമോണിയം നൈട്രേറ്റ് സ്ഫോടനത്തിൽ ഇരുപതാം നൂറ്റാണ്ടിന്റെ ആരംഭം മുതൽ നൂറുകണക്കിന് ആളുകൾ മരണപ്പെട്ടു.
ലഭ്യത
തിരുത്തുകഗ്വിഹാബൈറ്റ് എന്ന സ്വാഭാവിക ധാതു പോലെ അമോണിയം നൈട്രേറ്റ് കാണപ്പെടുന്നു. അമോണിയം നൈട്രേറ്റ് മുമ്പ് ഖനനം ചെയ്തിരുന്നു, എന്നാൽ ഇപ്പോൾ ഉപയോഗിക്കുന്ന രാസവസ്തുവിന്റെ 100% സിന്തറ്റിക് ആണ്.
ഉത്പാദനം, പ്രതികരണങ്ങൾ, സ്ഫടിക ഘട്ടങ്ങൾ
തിരുത്തുകനൈട്രിക് ആസിഡ് അമോണിയയുമായി പ്രതിപ്രവർത്തിപ്പിച്ച് അമോണിയം നൈട്രേറ്റിന്റെ വ്യാവസായിക ഉൽപാദനം നടത്തുന്നു.[5]
- HNO3 + NH3 → NH4 NO3
ഈ പ്രക്രിയയ്ക്ക് ആവശ്യമായ അമോണിയ നൈട്രജൻ, ഹൈഡ്രജൻ എന്നിവയിൽ നിന്ന് ഹേബർ പ്രക്രിയയിലൂടെ ലഭിക്കും. ഹേബർ പ്രക്രിയയിലൂടെ ഉത്പാദിപ്പിക്കപ്പെടുന്ന അമോണിയ ഓസ്റ്റ്വാൾഡ് പ്രക്രിയയിലൂടെ നൈട്രിക് ആസിഡിലേക്ക് ഓക്സീകരിക്കപ്പെടാം. നൈട്രോഫോസ്ഫേറ്റ് പ്രക്രിയയുടെ ഒരു വകഭേദമാണ് മറ്റൊരു ഉൽപാദന രീതി:
മെറ്റാറ്റിസിസ് പ്രതിപ്രവർത്തനങ്ങളിലൂടെയും അമോണിയം നൈട്രേറ്റ് ഉണ്ടാക്കാം:
- (NH4)2 SO4 + Ba(NO <sub id="mwWA">3</sub> ) <sub id="mwWQ">2</sub> → 2NH 4 NO3 + BaSO<sub id="mwXQ">4</sub>
- NH4Cl + AgNO3 → NH4NO3 + AgCl
പ്രതികരണങ്ങൾ
തിരുത്തുകഅമോണിയം നൈട്രേറ്റ് ഒരു ലവണം ആയതിനാൽ, കാറ്റേഷൻ, NH4+, അയോൺ, NO3 − എന്നിവ രാസപ്രവർത്തനങ്ങളിൽ പങ്കെടുക്കാം.
അമോണിയം നൈട്രേറ്റ് ലവണം ചൂടാക്കുമ്പോൾ വിഘടിപ്പിക്കുന്നു. 300° C ന് താഴെയുള്ള താപനിലയിൽ വിഘടിച്ച് പ്രധാനമായും നൈട്രസ് ഓക്സൈഡും ജലവും ഉൽപാദിപ്പിക്കുന്നു:
- NH4 NO3 → N2O + 2H2O.
ഉയർന്ന താപനിലയിൽ, ഇനിപ്പറയുന്ന പ്രതികരണം പ്രധാനമാണ്.
- 2NH4 NO3 → 2N2 + O2 + 4H2O.
വിഘടിപ്പിക്കുന്ന രണ്ട് പ്രതിപ്രവർത്തനങ്ങളും എക്സോതെർമിക് ആണ്, കൂടാതെ വാതക ഉൽപന്നങ്ങളുമുണ്ട്. ചില വ്യവസ്ഥകളിൽ, ഇത് സ്ഫോടനാത്മകമാകും. നിരവധി അമോണിയം നൈട്രേറ്റ് ദുരന്തങ്ങൾ ഉണ്ടായിട്ടുണ്ട്. ദ്വിതീയ പ്രതികരണ ഉൽപന്നമായ നൈട്രജൻ ഡൈ ഓക്സൈഡ് മൂലമാണ് സ്ഫോടനമേഘത്തിലെ തവിട്ട് നിറം ഉണ്ടാവുന്നത്.
ഉപയോഗങ്ങൾ
തിരുത്തുകഎൻപികെ റേറ്റിംഗ് 34-0-0 (34% നൈട്രജൻ) ഉള്ള ഒരു പ്രധാന വളമാണ് അമോണിയം നൈട്രേറ്റ്. [6] യൂറിയയേക്കാൾ അമോണിയം നൈട്രേറ്റിന്റെ ഗുണം അത് കൂടുതൽ സ്ഥിരതയുള്ളതും അന്തരീക്ഷത്തിലേക്ക് നൈട്രജൻ വേഗത്തിൽ നഷ്ടപ്പെടുന്നില്ല എന്നതുമാണ്.
സ്ഫോടകവസ്തുക്കൾ
തിരുത്തുകഅമോണിയം നൈട്രേറ്റ് സാധാരണയായി വിൽക്കുന്ന രൂപത്തിൽ ഒരു സ്ഫോടനാത്മകമല്ല. [7] എന്നിരുന്നാലും, അസൈഡുകൾ പോലുള്ള പ്രാഥമിക സ്ഫോടകവസ്തുക്കളുമായി അല്ലെങ്കിൽ അലുമിനിയം പൊടി അല്ലെങ്കിൽ ഇന്ധന എണ്ണ പോലുള്ള ഇന്ധനങ്ങളുമായി സംയോജിപ്പിക്കുമ്പോൾ വ്യത്യസ്ത സ്വഭാവങ്ങളുള്ള സ്ഫോടനാത്മക മിശ്രിതങ്ങൾ ഇത് പെട്ടെന്ന് സൃഷ്ടിക്കുന്നു.
ഇന്ധന എണ്ണയുമായി മിശ്രിതം
തിരുത്തുകANFO എന്നത് 94% അമോണിയം നൈട്രേറ്റ് (AN) 6% ഫ്വുവൽ ഓയിൽ എന്നിവ ചേർന്ന മിശ്രിതമാണ്. വ്യവസായ ആവശ്യങ്ങൾക്ക് സ്ഫോടകവസ്തുക്കളായി ഇത് വ്യാപകമായി ഉപയോഗിക്കുന്നു. [8] :1 കൽക്കരി ഖനനം, ക്വാറി, മെറ്റൽ ഖനനം, സിവിൽ നിർമ്മാണം എന്നിവയിൽ ഇത് ഉപയോഗിക്കുന്നു :2
തീവ്രവാദം
തിരുത്തുക1970 ലെ വിസ്കോൺസിൻ മാഡിസണിലെ സ്റ്റെർലിംഗ് ഹാൾ ബോംബാക്രമണം, 1995 ൽ ഒക്ലഹോമ സിറ്റി ബോംബാക്രമണം, 2011 ദില്ലി ബോംബാക്രമണം, 2011 ഓസ്ലോയിൽ നടന്ന ബോംബാക്രമണം, 2013 ഹൈദരാബാദ് സ്ഫോടനങ്ങൾ എന്നിവയിൽ അമോണിയം നൈട്രേറ്റ് അധിഷ്ഠിത സ്ഫോടകവസ്തുക്കൾ ഉപയോഗിച്ചു.
2009 നവംബറിൽ പാക്കിസ്ഥാനിലെ നോർത്ത് വെസ്റ്റ് ഫ്രോണ്ടിയർ പ്രവിശ്യ (എൻഡബ്ല്യുഎഫ്പി) സർക്കാർ സ്ഫോടകവസ്തുക്കൾ നിർമ്മിക്കാൻ തീവ്രവാദികൾ ഈ രാസവസ്തുക്കൾ ഉപയോഗിച്ചുവെന്ന റിപ്പോർട്ടിനെ തുടർന്ന് അമോണിയം സൾഫേറ്റ്, അമോണിയം നൈട്രേറ്റ്, കാൽസ്യം അമോണിയം നൈട്രേറ്റ് വളങ്ങൾ എന്നിവയ്ക്ക് നിരോധനം ഏർപ്പെടുത്തി [9]
സുരക്ഷ, കൈകാര്യം ചെയ്യൽ, സംഭരണം
തിരുത്തുകആരോഗ്യ, സുരക്ഷാഡാറ്റ വിതരണക്കാരിൽ നിന്ന് ലഭ്യമായ സുരക്ഷാ ഡാറ്റ ഷീറ്റുകളിൽ കാണിക്കുന്നുണ്ട്. [10] [11]
ചൂടാക്കൽ അല്ലെങ്കിൽ ഏതെങ്കിലും ജ്വലന ഉറവിടം അക്രമാസക്തമായ ജ്വലനത്തിനോ സ്ഫോടനത്തിനോ കാരണമായേക്കാം. [12] ശക്തമായ ഓക്സിഡന്റായതിനാൽ അമോണിയം നൈട്രേറ്റ്, ജ്വലനം കുറയ്ക്കുന്ന വസ്തുക്കളുമായി പ്രതിപ്രവർത്തിക്കുന്നു. ഇത് പ്രധാനമായും വളത്തിനായി ഉപയോഗിക്കുന്നുണ്ടെങ്കിലും സ്ഫോടകവസ്തുക്കൾക്കും ഉപയോഗിക്കാം. കാർഷിക കുളങ്ങൾ നിർമ്മിക്കാൻ ഇത് വെടിമരുന്നായി ഉപയോഗിച്ചിരുന്നു. [13] [14]
അമോണിയം നൈട്രേറ്റ് സംഭരിക്കുന്നതിനും കൈകാര്യം ചെയ്യുന്നതിനും നിരവധി സുരക്ഷാ മാർഗ്ഗനിർദ്ദേശങ്ങൾ ലഭ്യമാണ്. [15] ജ്വലന വസ്തുക്കൾക്ക് സമീപം ഇത് സൂക്ഷിക്കാൻ പാടില്ല. ക്ലോറേറ്റുകൾ, മിനറൽ ആസിഡുകൾ, മെറ്റൽ സൾഫൈഡുകൾ തുടങ്ങിയയുമായുള്ള സമ്പർക്കം ഊർജ്ജസ്വലമോ അക്രമാസക്തമോ ആയ വിഘടനത്തിന് കാരണമാകും. [16]
59.4% ആപേക്ഷിക ആർദ്രതയാണ് അമോണിയം നൈട്രേറ്റിന് ഉള്ളത്, അതിന് മുകളിൽ അന്തരീക്ഷത്തിൽ നിന്നുള്ള ഈർപ്പം ആഗിരണം ചെയ്യും. അതിനാൽ, കർശനമായി അടച്ച പാത്രത്തിൽ അമോണിയം നൈട്രേറ്റ് സൂക്ഷിക്കേണ്ടത് പ്രധാനമാണ്. അല്ലാത്തപക്ഷം, അത് ഒരു വലിയ, ഖര പിണ്ഡമായി യോജിക്കുന്നു. ദ്രവീകരിക്കാൻ ആവശ്യമായ ഈർപ്പം ആഗിരണം ചെയ്യാൻ അമോണിയം നൈട്രേറ്റിന് കഴിയും. മറ്റ് ചില രാസവളങ്ങളുമായി അമോണിയം നൈട്രേറ്റ് മിശ്രിതമാക്കുന്നത് ഗുരുതരമായ ആപേക്ഷിക ആർദ്രത കുറയ്ക്കും. [17]
മെറ്റീരിയൽ ഒരു സ്ഫോടകവസ്തുവായി ഉപയോഗിക്കുന്നതിനുള്ള സാധ്യത നിയന്ത്രണ നടപടികൾക്ക് കാരണമാകുന്നു. [18] ദുരുപയോഗം തടയുന്നതിന് ഉചിതമായ സുരക്ഷാ നടപടികളോടെ മാത്രമേ അപേക്ഷകർക്ക് വ്യവസായ ലൈസൻസുകൾ അനുവദിക്കൂ. [19] വിദ്യാഭ്യാസം, ഗവേഷണ ആവശ്യങ്ങൾ എന്നിവ പോലുള്ള അധിക ഉപയോഗങ്ങളും പരിഗണിക്കാമെങ്കിലും വ്യക്തിഗത ഉപയോഗം പരിഗണിക്കില്ല. ലഹരിവസ്തുക്കൾ കൈകാര്യം ചെയ്യുന്നതിനുള്ള ലൈസൻസുള്ള ജീവനക്കാർക്ക് ഇപ്പോഴും അംഗീകൃത ഉദ്യോഗസ്ഥരുടെ മേൽനോട്ടം ആവശ്യമാണ്.
ആരോഗ്യ അപകടങ്ങൾ
തിരുത്തുകമെറ്റീരിയൽ സുരക്ഷാ ഡാറ്റ ഷീറ്റുകളിൽ ആരോഗ്യവും സുരക്ഷാ ഡാറ്റയും കാണിച്ചിരിക്കുന്നു. അവ വിതരണക്കാരിൽ നിന്ന് ലഭ്യമാണ്, അവ ഇന്റർനെറ്റിൽ കണ്ടെത്താനും കഴിയും. [20]
അമോണിയം നൈട്രേറ്റ് ആരോഗ്യത്തിന് അപകടകരമല്ല, ഇത് സാധാരണയായി വളം ഉൽപന്നങ്ങളിൽ ഉപയോഗിക്കുന്നു. [20] [21]
അമോണിയം നൈട്രേറ്റിന് 2217 ന്റെ LD 50 ഉണ്ട് mg / kg, [22] ഇത് ടേബിൾ ഉപ്പിന്റെ മൂന്നിൽ രണ്ട് ഭാഗമാണ്.
ദുരന്തങ്ങൾ
തിരുത്തുകഅമോണിയം നൈട്രേറ്റ് സ്ഫോടനാത്മകമായി നൈട്രസ് ഓക്സൈഡ്, ചൂടാകുമ്പോൾ നീരാവി എന്നിവയിലേക്ക് വിഘടിപ്പിക്കുന്നു. പൊട്ടിത്തെറിയിലൂടെ സ്ഫോടനാത്മകമായി വിഘടിപ്പിക്കാൻ ഇത് പ്രേരിപ്പിക്കും. [23] മെറ്റീരിയലിന്റെ വലിയ സംഭരണികൾ അവയുടെ ഓക്സിഡേഷൻ കാരണം ഒരു വലിയ പൊട്ടിത്തെറിയിലേക്ക് എത്തിക്കും. വലിയതും വിനാശകരവുമായ നിരവധി സ്ഫോടനങ്ങൾ നടന്നിട്ടുണ്ട്. 1921 ലെ ഓപ്പാവു സ്ഫോടനം (ഏറ്റവും വലിയ കൃത്രിമ ആണവ ഇതര സ്ഫോടനങ്ങളിലൊന്ന് ), 1947 ലെ ടെക്സസ് സിറ്റി ദുരന്തം, 2015 ൽ ചൈനയിൽ നടന്ന ടിയാൻജിൻ സ്ഫോടനങ്ങൾ എന്നിവ ഉദാഹരണം. കൂടാതെ, 2020 ഓഗസ്റ്റ് 4 ന് ലെബനനിലെ ബെയ്റൂട്ടിലെ ഒരു തുറമുഖ വെയർഹൗസിൽ 2,750 ടൺ അമോണിയം നൈട്രേറ്റ് പൊട്ടിത്തെറിച്ചു.
ഇതുകൂടി കാണുക
തിരുത്തുകഅവലംബം
തിരുത്തുക- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. p. 362. ISBN 1-903996-65-1.
- ↑ "Archived copy". Archived from the original on 2015-02-17. Retrieved 2015-03-13.
{{cite web}}: CS1 maint: archived copy as title (link) - ↑ Karl-Heinz Zapp "Ammonium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry 2012, Wiley-VCH, Weinheim. doi:10.1002/14356007.a02_243
- ↑ "Archived copy" (PDF). Archived from the original (PDF) on 2012-01-23. Retrieved 2008-11-11.
{{cite web}}: CS1 maint: archived copy as title (link) - ↑ "Nutrient Content of Fertilizer Materials" (PDF). Archived from the original (PDF) on 2012-12-24. Retrieved 2012-06-27.
- ↑ Manhattan Bombs Provide Trove of Clues Archived 2020-06-20 at the Wayback Machine. – The New York Times
- ↑ Cook, Melvin A. (1974). The Science of Industrial Explosives. IRECO Chemicals. p. 1. ASIN B0000EGDJT.
- ↑ Brook, Tom Vanden. "Afghan bomb makers shifting to new explosives for IEDs". USA TODAY.
- ↑ "Ammonium nitrate MSDS". Archived from the original on 2011-08-18. Retrieved 2020-08-06.
- ↑ Chemical Advisory: Safe Storage, Handling, and Management of Ammonium Nitrate United States Environmental Protection Agency
- ↑ Pradyot Patnaik (2002). Handbook of Inorganic Chemicals. McGraw-Hill. ISBN 0-07-049439-8.
- ↑ "Pothole pond" (PDF). Archived from the original (PDF) on 2016-03-04. Retrieved 2020-08-06.
- ↑ Progressive Farmer Magazine
- ↑ "Storing and handling ammonium nitrate" (PDF). Archived from the original (PDF) on 2011-07-04. Retrieved 2006-03-22.
- ↑ "Chemical Engineering Transactions" (PDF). Archived from the original (PDF) on April 14, 2016.
- ↑ Fertilizers Europe (2006). "Guidance for Compatibility of Fertilizer Blending Materials" (PDF). Archived from the original (PDF) on 2015-06-08.
- ↑ "Dangerous Goods (HCDG) Regulations" (PDF).
- ↑ Ammonium Nitrate-Regulating its use, Balancing Access & Protection from "Worksafe Victoria". Archived from the original on 2011-03-11.
- ↑ 20.0 20.1 CF Industries. "Ammonium nitrate MSDS" (PDF). Archived from the original (PDF) on 2014-03-27.
- ↑ "Chemicalland21 – Ammonium Nitrate". Archived from the original on 2012-01-10.
- ↑ "Material Safety Data Sheet, Ammonium nitrate MSDS". Archived from the original on 2011-08-18. Retrieved 2020-08-06.
- ↑ Chaturvedi, Shalini; Dave, Pragnesh N. (January 2013). "Review on Thermal Decomposition of Ammonium Nitrate". Journal of Energetic Materials. 31 (1): 1–26. doi:10.1080/07370652.2011.573523.
ബാഹ്യ കണ്ണികൾ
തിരുത്തുക- International Chemical Safety Card 0216
- "അമോണിയം നൈട്രേറ്റ് സംഭരിക്കുകയും കൈകാര്യം ചെയ്യുകയും ചെയ്യുന്നു", യുണൈറ്റഡ് കിംഗ്ഡം ഹെൽത്ത് ആൻഡ് സേഫ്റ്റി എക്സിക്യൂട്ടീവ് പ്രസിദ്ധീകരണം INDG230 (1986)
- കെമിക്കൽ അഡ്വൈസറി: അമോണിയം നൈട്രേറ്റ് യുണൈറ്റഡ് സ്റ്റേറ്റ്സ് എൻവയോൺമെന്റൽ പ്രൊട്ടക്ഷൻ ഏജൻസിയുടെ സുരക്ഷിത സംഭരണം, കൈകാര്യം ചെയ്യൽ, കൈകാര്യം ചെയ്യൽ
- കാൽക്കുലേറ്ററുകൾ: ഉപരിതല പിരിമുറുക്കങ്ങളും Archived 2020-02-22 at the Wayback Machine. സാന്ദ്രത, Archived 2020-02-22 at the Wayback Machine. ജലീയ അമോണിയം നൈട്രേറ്റിന്റെ മോളാരിറ്റികളും മോളാലിറ്റികളും Archived 2020-02-22 at the Wayback Machine.
| HNO3 | He | ||||||||||||||||
| LiNO3 | Be(NO3)2 | B(NO 3)− 4 |
RONO2 | NO− 3 NH4NO3 |
HOONO2 | FNO3 | Ne | ||||||||||
| NaNO3 | Mg(NO3)2 | Al(NO3)3 | Si | P | S | ClONO2 | Ar | ||||||||||
| KNO3 | Ca(NO3)2 | Sc(NO3)3 | Ti(NO3)4 | VO(NO3)3 | Cr(NO3)3 | Mn(NO3)2 | Fe(NO3)2 Fe(NO3)3 |
Co(NO3)2 Co(NO3)3 |
Ni(NO3)2 | CuNO3 Cu(NO3)2 |
Zn(NO3)2 | Ga(NO3)3 | Ge | As | Se | Br | Kr |
| RbNO3 | Sr(NO3)2 | Y(NO3)3 | Zr(NO3)4 | Nb | Mo | Tc | Ru(NO3)3 | Rh(NO3)3 | Pd(NO3)2 Pd(NO3)4 |
AgNO3 Ag(NO3)2 |
Cd(NO3)2 | In | Sn | Sb(NO3)3 | Te | I | Xe(NO3)2 |
| CsNO3 | Ba(NO3)2 | Hf | Ta | W | Re | Os | Ir | Pt(NO3)2 Pt(NO3)4 |
Au(NO3)3 | Hg2(NO3)2 Hg(NO3)2 |
TlNO3 Tl(NO3)3 |
Pb(NO3)2 | Bi(NO3)3 BiO(NO3) |
Po(NO3)4 | At | Rn | |
| FrNO3 | Ra(NO3)2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| La(NO3)3 | Ce(NO3)3 Ce(NO3)4 |
Pr(NO3)3 | Nd(NO3)3 | Pm(NO3)3 | Sm(NO3)3 | Eu(NO3)3 | Gd(NO3)3 | Tb(NO3)3 | Dy(NO3)3 | Ho(NO3)3 | Er(NO3)3 | Tm(NO3)3 | Yb(NO3)3 | Lu(NO3)3 | |||
| Ac(NO3)3 | Th(NO3)4 | PaO2(NO3)3 | UO2(NO3)2 | Np(NO3)4 | Pu(NO3)4 | Am(NO3)3 | Cm(NO3)3 | Bk | Cf | Es | Fm | Md | No | Lr | |||