അസെറ്റോൺ
(Acetone എന്ന താളിൽ നിന്നും തിരിച്ചുവിട്ടതു പ്രകാരം)
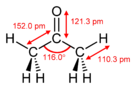
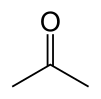
ഒരു ജൈവസംയുക്തമാണ് അസെറ്റോൺ (Acetone) അഥവാ പ്രൊപനോൺ (propanone). ഇതിന്റെ രാസസൂത്രം (CH3)2CO ആണ്.[15] നിറമില്ലാത്ത, ബാഷ്പീകരണശേഷിയുള്ള, കത്തുന്ന ഈ ദ്രാവകം ഏറ്റവും ലളിതവും ചെറുതുമായ കീറ്റോൺ ആണ്.
| |||
| |||

| |||
| Names | |||
|---|---|---|---|
| Preferred IUPAC name
Propan-2-one[7] | |||
| Other names | |||
| Identifiers | |||
3D model (JSmol)
|
|||
| 3DMet | |||
| Beilstein Reference | 635680 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.602 | ||
| EC Number |
| ||
| Gmelin Reference | 1466 | ||
| KEGG | |||
| MeSH | {{{value}}} | ||
PubChem CID
|
|||
| RTECS number |
| ||
| UNII | |||
| UN number | 1090 | ||
CompTox Dashboard (EPA)
|
|||
| InChI | |||
| SMILES | |||
| Properties | |||
| തന്മാത്രാ വാക്യം | |||
| Molar mass | 0 g mol−1 | ||
| Appearance | Colorless liquid | ||
| Odor | Pungent, irritating, floral, cucumber like | ||
| സാന്ദ്രത | 0.7845 g/cm3 (25 °C) | ||
| ദ്രവണാങ്കം | |||
| ക്വഥനാങ്കം | |||
| Miscible | |||
| Solubility | Miscible in benzene, diethyl ether, methanol, chloroform, ethanol[8] | ||
| log P | -0.16[9] | ||
| ബാഷ്പമർദ്ദം |
| ||
| അമ്ലത്വം (pKa) | |||
| −33.78·10−6 cm3/mol | |||
| Refractive index (nD) | 1.3588 (VD = 54.46) | ||
| വിസ്കോസിറ്റി | 0.295 mPa·s (25 °C)[8] | ||
| Structure | |||
| Trigonal planar at C2 | |||
| Dihedral at C2 | |||
| 2.91 D | |||
| Thermochemistry | |||
| Std enthalpy of formation ΔfH |
(−250.03) – (−248.77) kJ/mol | ||
| Std enthalpy of combustion ΔcH |
−1.772 MJ/mol | ||
| Standard molar entropy S |
200.4 J/(mol·K) | ||
| Specific heat capacity, C | 125.45 J/(mol·K) | ||
| Hazards | |||
| GHS pictograms |  
| ||
| GHS Signal word | Danger | ||
| H225, H319, H336, H373 | |||
| P210, P235, P260, P305+351+338 | |||
| Flash point | {{{value}}} | ||
| Explosive limits | 2.6–12.8%[13] | ||
Threshold limit value (TLV)
|
1185 mg/m3 (TWA), 2375 mg/m3 (STEL) | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (median dose)
|
| ||
LC50 (median concentration)
|
20,702 ppm (rat, 8 h)[14] | ||
LCLo (lowest published)
|
45,455 ppm (mouse, 1 h)[14] | ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
1000 ppm (2400 mg/m3)[6] | ||
REL (Recommended)
|
TWA 250 ppm (590 mg/m3)[6] | ||
IDLH (Immediate danger)
|
2500 ppm[6] | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
ജലത്തിൽ ലയിക്കുന്ന ഈ പദാർത്ഥം സ്വന്തം നിലയിലും നല്ലൊരു ലായകം ആണ്. 2010 -ൽ ഇതിന്റെ ഉൽപ്പാദനം 67 ലക്ഷം ടണ്ണോളം ആണ്. പ്രധാനമായും മീതൈൽ മെതാക്രിലേറ്റിന്റെയും ബൈസ്ഫിനോൾ ഏ യുടെയും നിർമ്മാണത്തിനാണ് അസെറ്റോൺ ഉപയോഗിക്കുന്നത്.[16][17] It is a common building block in organic chemistry. Familiar household uses of acetone are as the active ingredient in nail polish remover and as paint thinner. It has VOC exempt status in the USA[18].
അവലംബം
തിരുത്തുക- ↑ The Merck Index, 15th Ed. (2013), p. 13, Acetone Monograph 65, O'Neil: The Royal Society of Chemistry.(subscription required)
- ↑ 2.0 2.1 2.2 2.3 Acetone in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-05-11)
- ↑ Klamt, Andreas (2005). COSMO-RS: From Quantum Chemistry to Fluid Phase Thermodynamics and Drug Design. Elsevier. pp. 92–94. ISBN 978-0-444-51994-8.
- ↑ Ash, Michael; Ash, Irene (2004). Handbook of preservatives. Synapse Information Resources, Inc. p. 369. ISBN 1-890595-66-7.
- ↑ Myers, Richard L. (2007). The 100 Most Important Chemical Compounds: A Reference Guide. Greenwood. pp. 4–6. ISBN 978-0-313-08057-9.
- ↑ 6.0 6.1 6.2 6.3 "NIOSH Pocket Guide to Chemical Hazards #0260". National Institute for Occupational Safety and Health (NIOSH).
- ↑ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 723. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ 8.0 8.1 Properties of substance: acetone Archived 2014-05-12 at the Wayback Machine.. chemister.ru.
- ↑ "acetone". ChemSrc. Retrieved 2018-04-13.
- ↑ Chiang, Yvonne; Kresge, A. Jerry; Tang, Yui S.; Wirz, Jakob (1984). "The pKa and keto-enol equilibrium constant of acetone in aqueous solution". Journal of the American Chemical Society. 106 (2): 460–462. doi:10.1021/ja00314a055.
- ↑ Bordwell, Frederick G. (1988). "Equilibrium acidities in dimethyl sulfoxide solution". Accounts of Chemical Research. 21 (12): 456–463. doi:10.1021/ar00156a004.
- ↑ 12.0 12.1 Lide, David R. (ed) (2003). CRC Handbook of Chemistry and Physics, 84th Edition. CRC Press. Boca Raton, Florida; Section 3, Physical Constants of Organic Compounds.
- ↑ "Working with modern hydrocarbon and oxygenated solvents: a guide to flammability". American Chemistry Council Solvents Industry Group. January 2008. p. 7. Archived from the original on 2009-06-01.
- ↑ 14.0 14.1 14.2 "Acetone". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Allen, P.W.; Bowen, H.J.M.; Sutton, L.E.; Bastiansen, O. (1952). "The molecular structure of acetone". Transactions of the Faraday Society. 48: 991. doi:10.1039/TF9524800991.
- ↑ Acetone, World Petrochemicals report, January 2010
- ↑ Stylianos Sifniades, Alan B. Levy, "Acetone" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.
- ↑ "Update: U.S. EPA Exempt Volatile Organic Compounds". American Coatings Association (in അമേരിക്കൻ ഇംഗ്ലീഷ്). 2018-01-30. Archived from the original on 2021-02-08. Retrieved 2019-03-20.