സിൽവർ (I) ഓക്സൈഡ്
രാസസംയുക്തം
Ag2O എന്ന സൂത്രവാക്യമുള്ള രാസ സംയുക്തമാണ് സിൽവർ (I) ഓക്സൈഡ്. കറുത്ത, അല്ലെങ്കിൽ കടും തവിട്ട് നിറമുള്ള പൊടിയാണ് ഇത്. മറ്റ് വെള്ളി സംയുക്തങ്ങൾ തയ്യാറാക്കാൻ ഇത് ഉപയോഗിക്കുന്നു.
| |

| |
| Names | |
|---|---|
| IUPAC name
Silver(I) oxide
| |
| Other names
Silver rust, Argentous oxide, Silver monoxide
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.039.946 |
| EC Number |
|
| MeSH | {{{value}}} |
PubChem CID
|
|
| RTECS number |
|
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | Black/ brown cubic crystals |
| Odor | Odorless[1] |
| സാന്ദ്രത | 7.14 g/cm3 |
| ദ്രവണാങ്കം | |
| 0.013 g/L (20 °C) 0.025 g/L (25 °C)[2] 0.053 g/L (80 °C)[3] | |
Solubility product (Ksp) of AgOH
|
1.52·10−8 (20 °C) |
| Solubility | Soluble in acid, alkali Insoluble in ethanol[2] |
| −134.0·10−6 cm3/mol | |
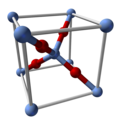
| Structure | |
| Cubic | |
| Pn3m, 224 | |
| Thermochemistry | |
| Std enthalpy of formation ΔfH |
−31 kJ/mol[5] |
| Standard molar entropy S |
122 J/mol·K[5] |
| Specific heat capacity, C | 65.9 J/mol·K[2] |
| Hazards | |
| GHS pictograms |   [6] [6]
|
| GHS Signal word | Danger |
| H272, H315, H319, H335[6] | |
| P220, P261, P305+351+338[6] | |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
2.82 g/kg (rats, oral)[1] |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
തയ്യാറാക്കൽ
തിരുത്തുകസിൽവർ നൈട്രേറ്റിന്റെയും ആൽക്കലി ഹൈഡ്രോക്സൈഡിന്റെയും ജലീയ ലായനി സംയോജിപ്പിച്ച് സിൽവർ ഓക്സൈഡ് തയ്യാറാക്കാം.[7] [8]
- 2 AgOH → Ag 2 O + H 2 O ( p <i id="mwPQ">K</i> = 2.875 [9] )
സവിശേഷതകൾ
തിരുത്തുകപല വെള്ളി സംയുക്തങ്ങളെയും പോലെ സിൽവർ ഓക്സൈഡും ഫോട്ടോസെൻസിറ്റീവ് ആണ്. 280 ന് മുകളിലുള്ള താപനിലയിലും ഇത് വിഘടിപ്പിക്കുന്നു . C. [10]
ഉപയോഗം
തിരുത്തുകഈ ഓക്സൈഡ് സിൽവർ-ഓക്സൈഡ് ബാറ്ററികളിൽ ഉപയോഗിക്കുന്നു. ഓർഗാനിക് കെമിസ്ട്രിയിൽ, സിൽവർ ഓക്സൈഡ് ഒരു ഓക്സിഡൈസിംഗ് ഏജന്റായി ഉപയോഗിക്കുന്നു. ഉദാഹരണത്തിന്, ഇത് ആൽഡിഹൈഡുകളെ കാർബോക്സിലിക് ആസിഡുകളിലേക്ക് ഓക്സിഡൈസ് ചെയ്യുന്നു.
അവലംബം
തിരുത്തുക- ↑ 1.0 1.1 1.2 "Silver Oxide MSDS". SaltLakeMetals.com. Salt Lake Metals. Retrieved 2014-06-08.
- ↑ 2.0 2.1 2.2 Lide, David R. (1998). Handbook of Chemistry and Physics (81 ed.). Boca Raton, FL: CRC Press. pp. 4–83. ISBN 0-8493-0594-2.
- ↑ 3.0 3.1 Perry, Dale L. (1995). Handbook of Inorganic Compounds (illustrated ed.). CRC Press. pp. 354. ISBN 0849386713.
- ↑ ഉദ്ധരിച്ചതിൽ പിഴവ്: അസാധുവായ
<ref>ടാഗ്;chemisterഎന്ന പേരിലെ അവലംബങ്ങൾക്ക് എഴുത്തൊന്നും നൽകിയിട്ടില്ല. - ↑ 5.0 5.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A23. ISBN 978-0-618-94690-7.
- ↑ 6.0 6.1 6.2 Sigma-Aldrich Co., Silver(I) oxide. Retrieved on 2014-06-07.
- ↑ O. Glemser and H. Sauer "Silver Oxide" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 1037.
- ↑ "4-Iodoveratrole", Org. Synth., 1963
- ↑ Biedermann, George; Sillén, Lars Gunnar (1960). "Studies on the Hydrolysis of Metal Ions. Part 30. A Critical Survey of the Solubility Equilibria of Ag2O". Acta Chemica Scandinavica. 13: 717. doi:10.3891/acta.chem.scand.14-0717.
- ↑ Merck Index of Chemicals and Drugs Archived 2009-02-01 at the Wayback Machine., 14th ed. monograph 8521