സിൽവർ കാർബണേറ്റ്
Ag 2CO3 എന്ന തന്മാത്രാസൂത്രത്തോടുകൂടിയ രാസ സംയുക്തമാണ് സിൽവർ കാർബണേറ്റ് . സിൽവർ കാർബണേറ്റ് മഞ്ഞയാണ്, പക്ഷേ മൂലക വെള്ളിയുടെ സാന്നിധ്യം കാരണം സാധാരണ സാമ്പിളുകൾ ചാരനിറമാണ്. മിക്ക സംക്രമണ ലോഹ കാർബണേറ്റുകളെയും പോലെ, ഇത് വെള്ളത്തിൽ ലയിക്കുന്നില്ല.
| |

| |
| Names | |
|---|---|
| IUPAC name
Silver(I) carbonate, Silver carbonate
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.007.811 |
| EC Number |
|
| MeSH | {{{value}}} |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | Pale yellow crystals |
| Odor | Odorless |
| സാന്ദ്രത | 6.077 g/cm3[1] |
| ദ്രവണാങ്കം | |
| 0.031 g/L (15 °C) 0.032 g/L (25 °C) 0.5 g/L (100 °C)[2] | |
Solubility product (Ksp)
|
8.46·10−12[1] |
| Solubility | Insoluble in alcohol, liquid ammonia, acetates, acetone[3] |
| −80.9·10−6 cm3/mol[1] | |
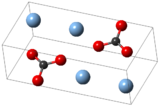
| Structure | |
| Monoclinic, mP12 (295 K) Trigonal, hP36 (β-form, 453 K) Hexagonal, hP18 (α-form, 476 K)[5] | |
| P21/m, No. 11 (295 K) P31c, No. 159 (β-form, 453 K) P62m, No. 189 (α-form, 476 K)[5] | |
| 2/m (295 K) 3m (β-form, 453 K) 6m2 (α-form, 476 K)[5] | |
a = 4.8521(2) Å, b = 9.5489(4) Å, c = 3.2536(1) Å (295 K)[5] α = 90°, β = 91.9713(3)°, γ = 90°
| |
| Thermochemistry | |
| Std enthalpy of formation ΔfH |
−505.8 kJ/mol[1] |
| Standard molar entropy S |
167.4 J/mol·K[1] |
| Specific heat capacity, C | 112.3 J/mol·K[1] |
| Hazards | |
| GHS pictograms |  [6] [6]
|
| GHS Signal word | Warning |
| H315, H319, H335[6] | |
| P261, P305+351+338[6] | |
| Inhalation hazard | Irritant |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
3.73 g/kg (mice, oral)[7] |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
തയ്യാറാക്കലും പ്രതികരണങ്ങളും
തിരുത്തുകസോഡിയം കാർബണേറ്റിന്റെ ജലീയ ലായനി സിൽവർ നൈട്രേറ്റിിന്റെ ജലിയ ലായനിയുമായി സംയോജിപ്പിച്ച് സിൽവർ കാർബണേറ്റ് തയ്യാറാക്കാം. [8]
- 2 AgNO 3 (aq) + Na 2 CO 3 (aq) → Ag 2 CO 3 (കൾ) + 2 NaNO 3 (aq)
പുതുതായി തയ്യാറാക്കിയ സിൽവർ കാർബണേറ്റ് നിറമില്ലാത്തതാണ്, പക്ഷേ ഈ ഖരപദാർത്ഥം പെട്ടെന്ന് മഞ്ഞയായി മാറുന്നു. [9]
സിൽവർ കാർബണേറ്റ് അമോണിയയുമായി പ്രതിപ്രവർത്തിച്ച് സ്ഫോടനാത്മക നിറത്തിലുള്ള വെള്ളി നൽകുന്നു . ഹൈഡ്രോഫ്ലൂറിക് ആസിഡ് ഉപയോഗിച്ച് ഇത് സിൽവർ ഫ്ലൂറൈഡ് നൽകുന്നു. സിൽവർ കാർബണേറ്റ് സിൽവർ ആയി പരിവർത്തനം ചെയ്യുന്നത് സിൽവർ ഓക്സൈഡിന്റെ രൂപവത്കരണത്തിലൂടെയാണ്: [10]
- Ag 2 CO 3 → Ag 2 O + CO 2
- 2Ag 2 O → 4 Ag + O 2
മൈക്രോഇലക്ട്രോണിക്സിൽ ഉപയോഗിക്കുന്നതിന് വെള്ളി പൊടി ഉൽപാദിപ്പിക്കുന്നതിനാണ് സിൽവർ കാർബണേറ്റിന്റെ പ്രധാന ഉപയോഗം. ഫോർമാൽഡിഹൈഡ് ഉപയോഗിച്ച് ക്ഷാര ലോഹങ്ങളില്ലാത്ത വെള്ളി ഉത്പാദിപ്പിക്കുകയും ചെയ്യുന്നു: [9]
അവലംബം
തിരുത്തുക- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 Lide, David R., ed. (2009). CRC Handbook of Chemistry and Physics (90th ed.). Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ↑ Seidell, Atherton; Linke, William F. (1919). Solubilities of Inorganic and Organic Compounds (2nd ed.). New York City: D. Van Nostrand Company. p. 605.
- ↑ Comey, Arthur Messinger; Hahn, Dorothy A. (February 1921). A Dictionary of Chemical Solubilities: Inorganic (2nd ed.). New York: The MacMillan Company. p. 203.
- ↑ ഉദ്ധരിച്ചതിൽ പിഴവ്: അസാധുവായ
<ref>ടാഗ്;chemisterഎന്ന പേരിലെ അവലംബങ്ങൾക്ക് എഴുത്തൊന്നും നൽകിയിട്ടില്ല. - ↑ 5.0 5.1 5.2 5.3 Norby, P.; Dinnebier, R.; Fitch, A.N. (2002). "Decomposition of Silver Carbonate; the Crystal Structure of Two High-Temperature Modifications of Ag2CO3". Inorganic Chemistry. 41 (14). doi:10.1021/ic0111177.
- ↑ 6.0 6.1 6.2 Sigma-Aldrich Co., Silver carbonate. Retrieved on 2014-05-06.
- ↑ 7.0 7.1 "Silver Carbonate MSDS". http://www.saltlakemetals.com. Salt Lake City, Utah: Salt Lake Metals. Retrieved 2014-06-08.
{{cite web}}: External link in|website= - ↑ McCloskey C. M.; Coleman, G. H. (1955), "β-d-Glucose-2,3,4,6-Tetraacetate", Org. Synth.; Coll. Vol., 3: 434
{{citation}}: Missing or empty|title=(help) - ↑ 9.0 9.1 Andreas Brumby et al. "Silver, Silver Compounds, and Silver Alloys" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2008. doi:10.1002/14356007.a24_107.pub2
- ↑ Koga, Nobuyoshi; Shuto Yamada; Tomoyasu Kimura (2013). "Thermal Decomposition of Silver Carbonate: Phenomenology and Physicogeometrical Kinetics". The Journal of Physical Chemistry C. 117: 326–336. doi:10.1021/jp309655s.
- ↑ J. Org. Chem., 2018, 83 (16), pp 9312–9321 DOI: 10.1021/acs.joc.8b01284. .