കണ്ടൻസേഷൻ റിയാക്ഷൻ
ഓർഗാനിക് കെമിസ്ട്രിയിൽ, ഒരു കണ്ടൻസേഷൻ റിയാക്ഷൻ എന്നത് രണ്ട് തന്മാത്രകൾ സംയോജിപ്പിച്ച് ഒരൊറ്റ തന്മാത്രയായി മാറുന്ന ഒരു തരം രാസപ്രവർത്തനമാണ്. അതിൽ, സാധാരണയായി ജലം, അമോണിയ, എത്തനോൾ, അസറ്റിക് ആസിഡ്, ഹൈഡ്രജൻ സൾഫൈഡ് തുടങ്ങിയ മറ്റ് തന്മാത്രകളും നഷ്ടപ്പെടാം. പോലുള്ള ഒരു ചെറിയ തന്മാത്രയുടെ നഷ്ടം. [1] ജലം നഷ്ടപ്പെടുകയാണെങ്കിൽ, പ്രതികരണത്തെ നിർജ്ജലീകരണ പ്രതികരണം എന്നും വിളിക്കുന്നു. [2]
പ്രതിപ്രവർത്തനത്തിൽ തന്മാത്രയുടെ പ്രവർത്തന ഗ്രൂപ്പുകൾ ഉൾപ്പെട്ടേക്കാം. ഒരു ഉൽപ്രേരകത്തിന്റെ സാന്നിധ്യത്തിൽ സംഭവിക്കാവുന്ന ഒരു ബഹുമുഖ പ്രതിപ്രവർത്തനമാണിത്. അമിനോ ആസിഡുകൾക്കിടയിലുള്ള പെപ്റ്റൈഡ് ബോണ്ടുകളുടെ രൂപീകരണത്തിനും ഫാറ്റി ആസിഡുകളുടെ ബയോസിന്തസിസിനും ഇത് അനിവാര്യമായതിനാൽ ഈ തരം പ്രതികരണങ്ങൾ സാധാരണമാണ്. [3] [4]
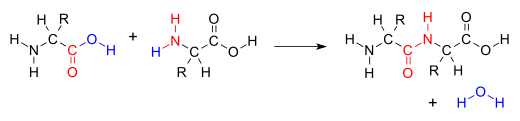
കണ്ടൻസേഷൻ പ്രതിപ്രവർത്തനങ്ങളുടെ പല വ്യതിയാനങ്ങളും നിലവിലുണ്ട്. ആൾഡോൾ കണ്ടൻസേഷൻ ജലം വിമുക്തമാക്കുന്നതും ക്ലെയ്സൻ കണ്ടൻസേഷൻ ഡയക്മാൻ കണ്ടൻസേഷൻ എന്നിവ ആൽക്കഹോൾ വിമുക്തമാക്കുന്നതുമാണ്.[5]
ഇതും കാണുക
തിരുത്തുകഅവലംബം
തിരുത്തുക- ↑ "25.18 Condensation Reactions". Book: Introductory Chemistry (CK-12). Chemistry Libre Texts. 12 August 2020. Retrieved 9 January 2021.
- ↑ "Condensation Reaction". IUPAC Compendium of Chemical Terminology (Gold Book). IUPAC. Retrieved 7 December 2017.
- ↑ Fakirov, S. (2019-02-01). "Condensation Polymers: Their Chemical Peculiarities Offer Great Opportunities". Progress in Polymer Science. 89: 1–18. doi:10.1016/j.progpolymsci.2018.09.003. ISSN 0079-6700.
- ↑ Voet, Donald; Voet, Judith; Pratt, Chriss (2008). Fundamentals of Biochemistry. Hoboken, NJ: John Wiley & Sons, Inc. pp. 88. ISBN 978-0470-12930-2.
- ↑ Bruckner, Reinhard (2002). Advanced Organic Chemistry (First ed.). San Diego, California: Harcourt Academic Press. pp. 414–427. ISBN 0-12-138110-2.