ആൽക്കെയ്ൻ
കാർബൺ (C) , ഹൈഡ്രജൻ (H) മൂലകങ്ങൾ മാത്രം അടങ്ങുന്നതും (ഹൈഡ്രോകാർബണുകൾ), ആറ്റങ്ങൾ ഏകബന്ധനം മുഖേന മാത്രം ബന്ധിപ്പിക്കപ്പെട്ടിരിക്കുന്നതും (പൂരിത സംയുക്തങ്ങൾ), ചാക്രിക ഘടനയില്ലാത്തതുമായ രാസസംയുക്തങ്ങളാണ് ആൽക്കെയ്നുകൾ. പാരഫിനുകൾ എന്നും ഇവയെ വിളിക്കുന്നു. ആൽക്കെയ്നുകൾ ഓർഗാനിക് സംയുക്തങ്ങളുടെ ഒരു ഹോമോലോഗസ് പരമ്പരയിൽ ഉൾപ്പെടുന്നു. ഇതിലെ അടുത്തടുത്തുള്ള അംഗങ്ങൾ തമ്മിൽ 14 അണുഭാരം വ്യത്യാസമുണ്ടായിരിക്കും.
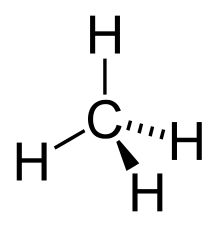
ഓരോ കാർബൺ ആറ്റത്തിനും 4 ബന്ധനങ്ങൾ ഉണ്ടായിരിക്കും (C-H അല്ലെങ്കിൽ C-C ബന്ധനം). ഓരോ ഹൈഡ്രജൻ ആറ്റവും ഒരു കാർബൺ ആറ്റവുമായി ബന്ധിക്കപ്പെട്ടിരിക്കും. പരസ്പരം ബന്ധിക്കപ്പെട്ടിരിക്കുന്ന കാർബണുകളുടെ ഒരു പരമ്പരയെ കാർബൺ നട്ടെല്ല് അല്ലെങ്കിൽ കാർബൺ ചങ്ങല എന്ന് വിളിക്കുന്നു. സാധാരണയായി ഒരു ആൽക്കെയ്നിലെ കാർബൺ ആറ്റങ്ങളുടെ എണ്ണമാണ് അതിന്റെ വലിപ്പം നിർണയിക്കാൻ ഉപയോഗിക്കുന്നത്.
ആൽക്കൈൽ ഗ്രൂപ്പ് എന്നത് ഒരു ഫങ്ഷണൽ ഗ്രൂപ്പ് അഥവാ ശാഖയാണ്. ആൽക്കെയ്നുകളേപ്പോലെതന്നെ ഏകബന്ധനം വഴി ബന്ധിക്കപ്പെട്ടിരിക്കുന്ന കാർബണും ഹൈഡ്രജനും മാത്രമാണ് ആൽക്കൈൽ ഗ്രൂപ്പിലെ ഘടകങ്ങൾ. മെഥൈൽ, എഥൈൽ ഗ്രൂപ്പുകൾ ഇതിന് ഉദാഹരണങ്ങളാണ്.
പൂരിത ഹൈഡ്രോകാർബണുകൾ 3 ഘടനകളിൽ കാണപ്പെടുന്നു. രേഖീയ ഘടനയിൽ കാർബൺ ആറ്റങ്ങൾ പാമ്പിന്റെ രൂപത്തിനു സമാനമായ രീതിയിൽ ബന്ധിക്കപ്പെട്ടിരിക്കും (പൊതു സൂത്രവാക്യം CnH2n+2). ശാഖാ ഘടനയിൽ കാർബൺ ചങ്ങല ഒന്നോ അതിലധികമോ ഭാഗങ്ങളിൽ പല ദിശകളിലേക്ക് വേർപിരിയും(പൊതു സൂത്രവാക്യം CnH2n+2, n>3). ചാക്രിക ഘടനയിൽ കാർബൺ ആറ്റങ്ങൾ വൃത്ത രൂപത്തിലായിരിക്കും ബന്ധിക്കപ്പെട്ടിരിക്കുന്നത് (പൊതു സൂത്രവാക്യം CnH2n, n>2). ഐ.യു.പി.എ.സി-യുടെ നിർവചനം അനുസരിച്ച് ഇതിൽ ആദ്യത്തെ രണ്ടെണ്ണം ആൽക്കെയ്നുകളും മൂന്നാമത്തേത് ചാക്രികആൽക്കെയ്നുമാണ് (സൈക്ലോആൽക്കെയ്ൻ). അതായത്, പൂരിത ഹൈഡ്രോകാർബണുകളെ ആൽക്കെയ്നുകളെന്നും സൈക്ലോആൽക്കെയ്നുകളെന്നും വിഭാഗിച്ചിരിക്കുന്നു. സാങ്കേതികമായി സക്ലോആൽക്കെയ്നുകൾ ആൽക്കെയ്നുകളല്ല. സക്ലോആൽക്കെയ്നുകളെ സൈക്ലിക് ആൽക്കെയ്നുകളെന്നും വിളിക്കുന്നു.
സൃഷ്ടിക്കാനാവുന്നതിൽ ഏറ്റവും ലളിതമായ ആൽക്കെയ്ൻ മീഥെയ്ൻ ആണ്. ബന്ധനത്തിലേർപ്പെടാവുന്ന കാർബണുകളുടെ എണ്ണത്തിന് പരിധിയില്ല. തന്മാത്ര ഒരു ഹൈഡ്രോകാർബണും അചാക്രികവും അപൂരിതവുമായിരിക്കണമെന്നത് മാത്രമാണ് ഒരു ആൽക്കെയ്നാകുന്നതിനുള്ള നിബന്ധനകൾ. അപൂരിത എണ്ണകളും മെഴുകുകളും വലിയ അപൂരിത ഹൈഡ്രോകാർബണുകൾക്ക് ഉദാഹരണങ്ങളാണ്. ഇവയിൽ പ്രധാന കാർബൺ ചങ്ങലയിലെ കാർബണുകളുടെ എണ്ണം മിക്കപ്പോഴും 10-നേക്കാൾ അധികമായിരിക്കും.
ആൽക്കെയ്നുകൾ ക്രീയാശീലം വളരെ കുറഞ്ഞവയും കുറച്ച് ജൈവിക പ്രവർത്തനങ്ങൾ മാത്രമുള്ളവയുമാണ്.
ഐസോമെറിസം
തിരുത്തുകമൂന്നിലധികം കാർബണുകളുള്ള ആൽക്കെയ്നുകളെ പല രീതിയിൽ ക്രമീകരിക്കാനാകും. ഘടനാ ഐസോമെറുകളുടെ രൂപവത്കരണത്തിന് ഇത് കാരണമാകുന്നു. കാർബൺ ആറ്റങ്ങൾ ഏകബന്ധനം വഴി ബന്ധിക്കപ്പെട്ടിരിക്കുന്നതും ശാഖകളില്ലാത്തതുമായ ഘടനയാണ് ഒരു ആൽക്കെയ്നിന്റെ ഏറ്റവും ലളിതമായ ഐസോമെർ. ഇതിനെ n-ഐസോമെർ എന്ന് വിളിക്കാറുണ്ട്. എന്നാൽ കാർബൺ ചങ്ങല ഒന്നോ അതിലധികമോ ഇടങ്ങളിൽ ശാഖകളുള്ളതുമാകാം. ചങ്ങലയിലെ കാർബണുകളുടെ എണ്ണം കൂടുന്നതിനനുസരിച്ച് സാധ്യമായ ഐസോമെറുകളുടെ എണ്ണവും കൂടുന്നു. ഉദാഹരണമായി:
- C1: 1 ഐസോമെർ—മീഥെയ്ൻ
- C2: 1 ഐസോമെർ—ഈഥെയ്ൻ
- C3: 1 ഐസോമെർ—പ്രൊപ്പെയ്ൻ
- C4: 2 ഐസോമെറുകൾ—n-ബ്യൂട്ടെയ്ൻ, ഐസോബ്യൂട്ടെയ്ൻ
- C12: 355 ഐസോമെറുകൾ
- C32: 27,711,253,769 ഐസോമെറുകൾ
- C60: 22,158,734,535,770,411,074,184 ഐസോമെറുകൾ, ഇവയിൽ പലതും സ്ഥിരതയില്ലാത്തവയാണ്.