കാൽസ്യം ബൈകാർബണേറ്റ്
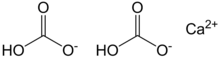
കാൽസ്യം ഹൈഡ്രജൻ കാർബണേറ്റ് എന്നും വിളിക്കപ്പെടുന്ന ഒരു കാൽസ്യം സംയുക്തമാണ് കാൽസ്യം ബൈകാർബണേറ്റ്. ഇതിന്റെ രാസ സൂത്രം Ca(HCO3)2. ഇത് ഖരസംയുക്തമായി കാണപ്പെടുന്നില്ല. കാൽസ്യം (Ca 2+ ), ബൈകാർബണേറ്റ് ( HCO−
3 ) അയോണുകളായി ജലീയ ലായനിയിൽ മാത്രമേ ഇത് നിലനിൽക്കൂ. കാർബണേറ്റ് ( CO2−
3 ) അയോണുകൾ, ജലത്തിൽ ലയിച്ചരൂപത്തിൽ കാർബൺ ഡൈ ഓക്സൈഡ് (CO 2 ) എന്നിവയോടൊപ്പമാണ് ലഭ്യമാവുക.
| |
| Names | |
|---|---|
| IUPAC name
Calcium hydrogen carbonate
| |
| Other names
Cleansing lime
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| 16.1 g/100 mL (0 °C) 16.6 g/100 mL (20 °C) 18.4 g/100 mL (100 °C) | |
| Hazards | |
| Main hazards | Irritant |
| Flash point | {{{value}}} |
| Related compounds | |
| Other cations | Magnesium bicarbonate |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
അന്തരീക്ഷവുമായി സമ്പർക്കം പുലർത്തുന്ന ജലം കാർബൺ ഡൈ ഓക്സൈഡിനെ ആഗിരണം ചെയ്യുന്നു. ഈ ജലം പാറകളുമായും അവശിഷ്ടങ്ങളുമായും സമ്പർക്കം പുലർത്തുന്നതിനാൽ അവ സാധാരണയായി കാൽസ്യം, മഗ്നീഷ്യം തുടങ്ങിയവയുടെ ലോഹ അയോണുകൾ സ്വീകരിക്കുന്നു. അതിനാൽ അരുവികൾ, തടാകങ്ങൾ, പ്രത്യേകിച്ച് കിണറുകൾ എന്നിവയിൽ നിന്ന് വരുന്ന പ്രകൃതിദത്ത ജലം ഈ ബൈകാർബണേറ്റുകളുടെ നേർപ്പിച്ച ലായനിയായി കണക്കാക്കുന്നു. ഈ കഠിന ജലം പൈപ്പുകളിലും ബോയിലറുകളിലും കാർബണേറ്റ് പാളി ഉണ്ടാക്കുന്നു. അവ സോപ്പുകളുമായി പ്രതിപ്രവർത്തിച്ച് അഭികാമ്യമല്ലാത്ത മലിനജലമുണ്ടാക്കുന്നു.
കാൽസ്യം ബൈകാർബണേറ്റിന്റെ ലായനിയെ ബാഷ്പീകരിച്ചുകൊണ്ട് ഖരസംയുക്തം തയ്യാറാക്കാൻ സാധ്യമല്ല. ഇങ്ങനെ ചെയ്യുമ്പോൾ, കാൽസ്യം കാർബണേറ്റ് ആണ് പകരമായി ഉണ്ടാവുന്നത്: [1]
അവലംബം
തിരുത്തുക- ↑ "ആർക്കൈവ് പകർപ്പ്". Archived from the original on 2015-02-26. Retrieved 2021-01-05.