സിൽവർ (I) ഓക്സൈഡ്
രാസസംയുക്തം
(Silver oxide എന്ന താളിൽ നിന്നും തിരിച്ചുവിട്ടതു പ്രകാരം)
Ag2O എന്ന സൂത്രവാക്യമുള്ള രാസ സംയുക്തമാണ് സിൽവർ (I) ഓക്സൈഡ്. കറുത്ത, അല്ലെങ്കിൽ കടും തവിട്ട് നിറമുള്ള പൊടിയാണ് ഇത്. മറ്റ് വെള്ളി സംയുക്തങ്ങൾ തയ്യാറാക്കാൻ ഇത് ഉപയോഗിക്കുന്നു.
| |

| |
| Names | |
|---|---|
| IUPAC name
Silver(I) oxide
| |
| Other names
Silver rust, Argentous oxide, Silver monoxide
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.039.946 |
| EC Number |
|
| MeSH | {{{value}}} |
PubChem CID
|
|
| RTECS number |
|
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
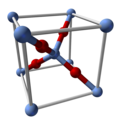
| Appearance | Black/ brown cubic crystals |
| Odor | Odorless[1] |
| സാന്ദ്രത | 7.14 g/cm3 |
| ദ്രവണാങ്കം | |
| 0.013 g/L (20 °C) 0.025 g/L (25 °C)[2] 0.053 g/L (80 °C)[3] | |
Solubility product (Ksp) of AgOH
|
1.52·10−8 (20 °C) |
| Solubility | Soluble in acid, alkali Insoluble in ethanol[2] |
| −134.0·10−6 cm3/mol | |
| Structure | |
| Cubic | |
| Pn3m, 224 | |
| Thermochemistry | |
| Std enthalpy of formation ΔfH |
−31 kJ/mol[5] |
| Standard molar entropy S |
122 J/mol·K[5] |
| Specific heat capacity, C | 65.9 J/mol·K[2] |
| Hazards | |
| GHS pictograms |   [6] [6]
|
| GHS Signal word | Danger |
| H272, H315, H319, H335[6] | |
| P220, P261, P305+351+338[6] | |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
2.82 g/kg (rats, oral)[1] |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
തയ്യാറാക്കൽ
തിരുത്തുകസിൽവർ നൈട്രേറ്റിന്റെയും ആൽക്കലി ഹൈഡ്രോക്സൈഡിന്റെയും ജലീയ ലായനി സംയോജിപ്പിച്ച് സിൽവർ ഓക്സൈഡ് തയ്യാറാക്കാം.[7] [8]
- 2 AgOH → Ag 2 O + H 2 O ( p <i id="mwPQ">K</i> = 2.875 [9] )
സവിശേഷതകൾ
തിരുത്തുകപല വെള്ളി സംയുക്തങ്ങളെയും പോലെ സിൽവർ ഓക്സൈഡും ഫോട്ടോസെൻസിറ്റീവ് ആണ്. 280 ന് മുകളിലുള്ള താപനിലയിലും ഇത് വിഘടിപ്പിക്കുന്നു . C. [10]
ഉപയോഗം
തിരുത്തുകഈ ഓക്സൈഡ് സിൽവർ-ഓക്സൈഡ് ബാറ്ററികളിൽ ഉപയോഗിക്കുന്നു. ഓർഗാനിക് കെമിസ്ട്രിയിൽ, സിൽവർ ഓക്സൈഡ് ഒരു ഓക്സിഡൈസിംഗ് ഏജന്റായി ഉപയോഗിക്കുന്നു. ഉദാഹരണത്തിന്, ഇത് ആൽഡിഹൈഡുകളെ കാർബോക്സിലിക് ആസിഡുകളിലേക്ക് ഓക്സിഡൈസ് ചെയ്യുന്നു.
അവലംബം
തിരുത്തുക- ↑ 1.0 1.1 1.2 "Silver Oxide MSDS". SaltLakeMetals.com. Salt Lake Metals. Retrieved 2014-06-08.
- ↑ 2.0 2.1 2.2 Lide, David R. (1998). Handbook of Chemistry and Physics (81 ed.). Boca Raton, FL: CRC Press. pp. 4–83. ISBN 0-8493-0594-2.
- ↑ 3.0 3.1 Perry, Dale L. (1995). Handbook of Inorganic Compounds (illustrated ed.). CRC Press. pp. 354. ISBN 0849386713.
- ↑ ഉദ്ധരിച്ചതിൽ പിഴവ്: അസാധുവായ
<ref>ടാഗ്;chemisterഎന്ന പേരിലെ അവലംബങ്ങൾക്ക് എഴുത്തൊന്നും നൽകിയിട്ടില്ല. - ↑ 5.0 5.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A23. ISBN 978-0-618-94690-7.
- ↑ 6.0 6.1 6.2 Sigma-Aldrich Co., Silver(I) oxide. Retrieved on 2014-06-07.
- ↑ O. Glemser and H. Sauer "Silver Oxide" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 1037.
- ↑ "4-Iodoveratrole", Org. Synth., 1963
- ↑ Biedermann, George; Sillén, Lars Gunnar (1960). "Studies on the Hydrolysis of Metal Ions. Part 30. A Critical Survey of the Solubility Equilibria of Ag2O". Acta Chemica Scandinavica. 13: 717. doi:10.3891/acta.chem.scand.14-0717.
- ↑ Merck Index of Chemicals and Drugs Archived 2009-02-01 at the Wayback Machine., 14th ed. monograph 8521